ทำลายอุปสรรคในช่องปาก (4)
Feb 05, 2026
การค้นพบและการเกิดอนุพันธ์ของไซคลิกเปปไทด์ PTG-200
การค้นพบ PTG-200
ในปี 2016 ตัวเอกเปิดเผยสิทธิบัตร (WO2016011208) สำหรับตัวยับยั้งโพลีเปปไทด์แบบรับประทานซึ่งกำหนดเป้าหมาย IL-23R ซึ่งรวมถึงลำดับเปปไทด์เชิงเส้นและไซคลิกหลายลำดับที่สามารถจับกับ IL-23R ลำดับที่นำเสนอในตารางที่ 3A ของสิทธิบัตรนี้มีความคล้ายคลึงอย่างใกล้ชิดกับโครงสร้างที่ได้รับก่อนหน้านี้โดย MDL ผ่านการแสดงฟาจ ลำดับเปปไทด์เชิงเส้นที่แสดงไว้โดยหลักแล้วมีโครงสร้างแกนกลาง -WQDYW- (ดังแสดงในรูปด้านล่าง) ในบรรดาโมเลกุลเหล่านั้น โมเลกุลที่มีศักยภาพมากที่สุด (SEQ ID NO.4) มีความเข้มข้นในการยับยั้ง IL-23R ที่ 4.1 µM โดยมีโครงสร้างของมันเกิดขึ้นจากอะซิติเลตปลาย N ของเปปไทด์ 23.15 ของ MDL
เป็นที่น่าสังเกตว่าครั้งหนึ่ง MDL และตัวละครเอกเคยเจรจาความร่วมมือเกี่ยวกับเปปไทด์ IL-23R ในปี 2014 ซึ่งในระหว่างนั้น MDL ได้แบ่งปันข้อมูลการวิจัยของตน ในปี 2558 ทั้งสองฝ่ายได้ลงนามในข้อตกลงการรักษาความลับ แต่การเจรจาสิ้นสุดลงในเดือนตุลาคมของปีเดียวกัน เอกสารทางกฎหมายที่ตามมาเผยให้เห็นว่า MDL ได้ยื่นฟ้อง Protagonist ในศาลแขวงสหรัฐฯ โดยกล่าวหาว่า PTG-200 ละเมิดสิทธิบัตร ซึ่งเกี่ยวข้องกับสิทธิบัตร US 8946150 (MDL) และ US 9624268 (ตัวเอก) ในปี 2018 การเรียกร้องการละเมิดสิทธิบัตรของ MDL ถูกยกเลิกเนื่องจากตัวเอกใช้เปปไทด์เหล่านี้เพื่อพัฒนายาที่ได้รับการอนุมัติจาก FDA สำหรับโรคแพ้ภูมิตัวเอง ซึ่งได้รับการคุ้มครองภายใต้กฎ Safe Harbor
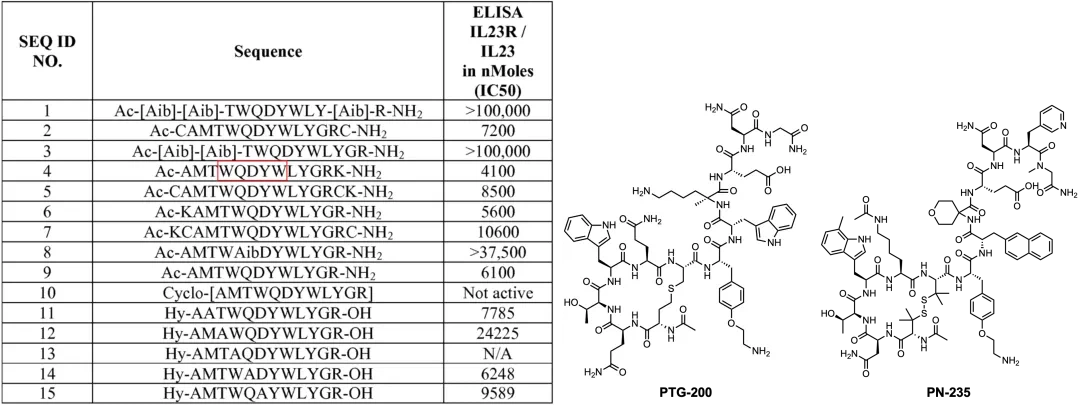
เมื่อกลับมาที่จุดเน้นของบทความนี้ ตัวเอกยังคงรักษาโครงสร้างหลัก WQDYW - ที่เสนอโดย MDL ในการดัดแปลงโมเลกุลในเวลาต่อมา แต่นำการออกแบบที่แตกต่างกันมาใช้ในกลยุทธ์การหมุนเวียน พวกเขาแนะนำ Cys เข้าไปในลำดับแกนกลางเพื่อสร้างโครงสร้างอนุรักษ์ - CXX-WQCYW - (เช่น - CQTWQCYW -) และได้รับเปปไทด์หลายร้อยเปปไทด์รอบๆ โครงสร้างนี้ ซึ่งเพิ่มกิจกรรมจนถึงระดับนาโนโมลาร์ (ดังแสดงในแผนภาพด้านล่าง) นอกจากนี้ ตัวเอกยังได้ลองวิธีการไซโคลไลเซชันหลายวิธี รวมถึงการแนะนำพันธะไทโออีเทอร์ระหว่างไซต์ Cys สองแห่ง โดยใช้ปฏิกิริยาโอเลฟินเมทาทิซิส (RCM) และการนำกลยุทธ์การไซคลิกไลเซชันของพันธะเอไมด์ไปใช้ อย่างไรก็ตาม ผลการทดลองบ่งชี้ว่าเปปไทด์แบบไซคลิกโดยพันธะไดซัลไฟด์หรือไทโออีเทอร์โดยทั่วไปแสดงฤทธิ์ได้ดีกว่าเปปไทด์แบบไซคลิกโดย RCM หรือพันธะเอไมด์
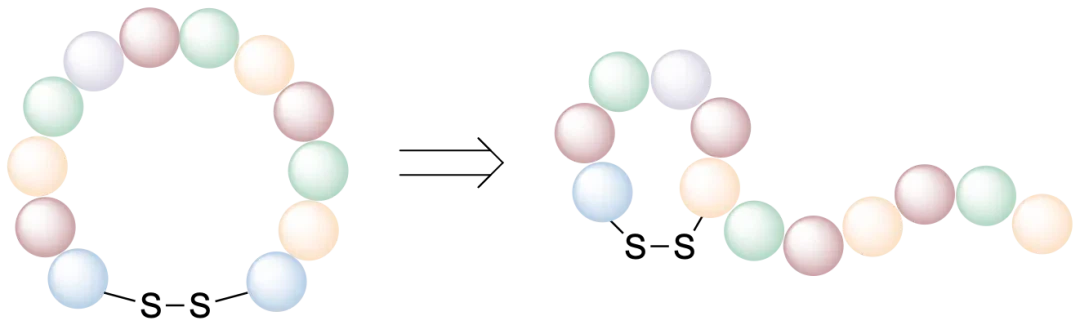
ข้อมูล PK ของ PTG-200 (สารประกอบ C) ได้รับการเปิดเผยในสิทธิบัตร: หลังจากให้หนูทดลองทางปากด้วยขนาด 20 มก./กก. สารประกอบส่วนใหญ่จะถูกกระจายในเนื้อเยื่อของระบบทางเดินอาหาร โดยมีการสัมผัสทั่วร่างกายต่ำมาก ในหมู่พวกเขา AUC ของเยื่อเมือกในลำไส้เล็กคือ 355 μ g · h/g และค่า AUC ของเยื่อบุลำไส้คือ 77 μ g · h/g อย่างไรก็ตาม AUC ในพลาสมามีค่าเพียง 0.3 μ g · h/mL โดยมีอัตราการฟื้นตัวในอุจจาระอยู่ที่ 40% สารประกอบนี้มีความคงตัวที่ดีในของเหลวในทางเดินอาหารต่างๆ และสภาพแวดล้อมแบบรีดิวซ์: ครึ่ง-ชีวิตของมันมากกว่า 24 ชั่วโมงในน้ำในลำไส้จำลอง (SIF), น้ำในกระเพาะอาหารจำลอง (SGF) และของเหลวในลำไส้ของมนุษย์ และยังมีครึ่งชีวิตนานกว่า 2 ชั่วโมงในสารรีดิวซ์ DTT ผลการทดลอง SPR แสดงให้เห็นว่ามันไม่ได้จับกับ IL-12R 1 เพียงอย่างเดียว แต่สามารถจับกับพื้นผิวของ IL-23R และ IL-12R 1/IL-23R ที่ถูกแสดงออกร่วมกันด้วยสัมพรรคภาพที่แข็งแกร่งและค่า KD ที่ 2.42 นาโนโมลาร์ และ 2.56 นาโนโมลาร์ ตามลำดับ
อนุพันธ์ของ PTG-200
ในปี 2017 ตัวเอกได้ตีพิมพ์สิทธิบัตรฉบับที่สองสำหรับสารยับยั้งเปปไทด์ IL-23R (WO2017011820) สิทธิบัตรนี้ขยายโครงร่างของสิทธิบัตรแรกด้วยลำดับที่ได้รับมา 227 ลำดับ (SEQ ID NO.1030-1256) และแนะนำหน่วยโครงสร้างบนเปปไทด์แบบไซคลิกที่สามารถยืดอายุครึ่งชีวิต ภายในร่างกาย ได้ (ดังแสดงในรูปต่อไปนี้) การศึกษาทางเภสัชจลนศาสตร์แสดงให้เห็นว่าหลังจากให้เปปไทด์ NO.1185 ขนาด 10 มก./กก. แก่หนู ความเข้มข้นในพลาสมาจะต่ำกว่าความเข้มข้นในตัวอย่างลำไส้เล็กและลำไส้ใหญ่อย่างมาก และอัตราการฟื้นตัวของอุจจาระจะสูงถึง 20% หลังจาก 24 ชั่วโมง การประเมินความปลอดภัยแสดงให้เห็นว่าเปปไทด์ NO.1185 ไม่แสดงผลการยับยั้งต่อเป้าหมาย 44 รายการ รวมถึงตัวรับควบคู่กับโปรตีน G ตัวขนส่ง และช่องไอออนที่ 10 µM
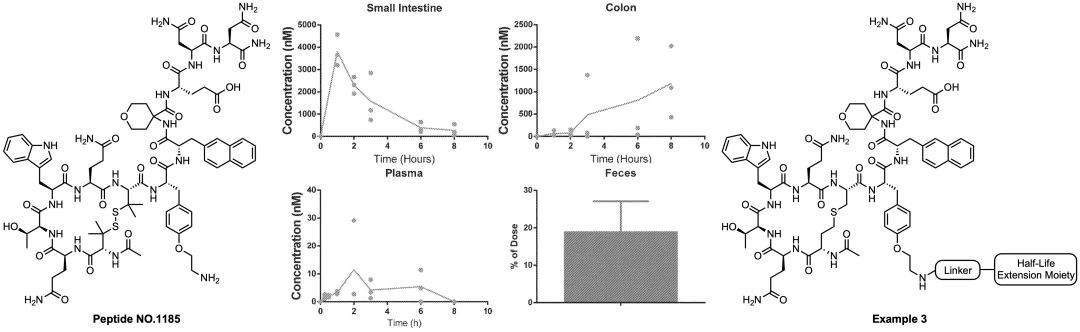
ต่อมา ตัวเอกได้เผยแพร่สิทธิบัตรอนุพันธ์หลายฉบับโดยใช้โครงสร้าง PTG-200 หรือเปปไทด์ NO.1185 ซึ่งปรับปรุงกิจกรรมและความเสถียรให้เหมาะสมยิ่งขึ้นผ่านการดัดแปลงโครงสร้างที่จุดตกค้างต่างๆ รายละเอียดของการแก้ไขที่เกี่ยวข้องสามารถดูได้ในสิทธิบัตร WO2018136646, WO2020014646, WO2021007433 และ WO2021146458 นอกจากนี้ ตัวเอกยังได้ยื่นขอสิทธิบัตร (WO2018022937) ที่ครอบคลุมตัวยับยั้งไซคลิกเปปไทด์ IL-23R ที่มีกรดอะมิโน 34 ตัว ซึ่งจะไม่มีการกล่าวถึงเพิ่มเติมในบทความนี้








